5G賦能工業安全 寶山企業智慧監控系統入選國家能源局優秀案例

國家能源局公布了2023年度5G應用優秀案例名單,其中,由上海寶山區某科技企業自主研發并實施的“基于5G網絡的工業安全智能監控與預警系統”成功入選,成為工業互聯網與能源安全領域融合創新的標桿案例。這一榮譽不僅彰顯了企業在5G+工業互聯網應用領域的領先實力,也為全國能源行業的智能化安全管控提供了可復制的“寶山方案”。
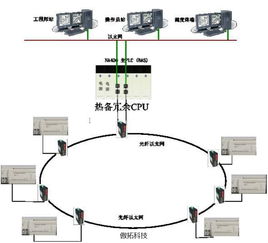
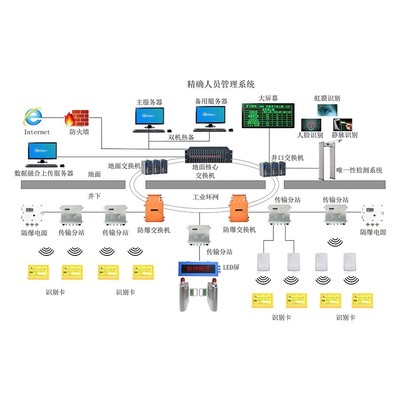
該案例的核心,是構建了一套深度融合5G通信、物聯網、邊緣計算與人工智能的工業安全監控服務體系。系統針對能源行業(如電廠、變電站、油氣管道、礦山等)高危復雜環境下的安全生產痛點,實現了三大突破性應用:
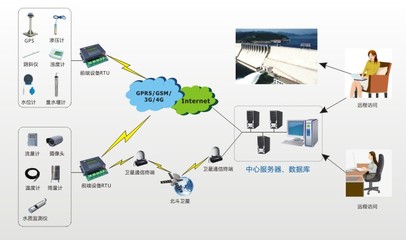
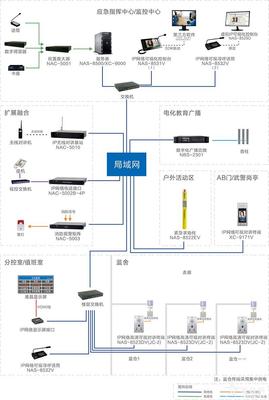
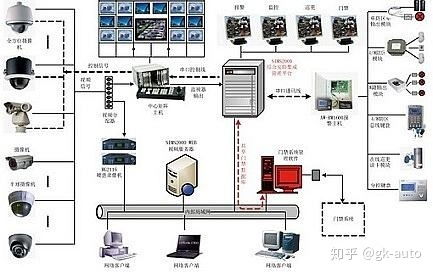
一、全場景、無死角的實時高清監控。借助5G網絡大帶寬、低時延的特性,系統在廠區、作業面、關鍵設備等區域部署了超高清視頻采集終端,將畫質提升至4K/8K級別,并能通過5G網絡實時、穩定地回傳至云端或邊緣計算中心。管理人員可隨時隨地通過多終端調閱現場畫面,實現對生產全流程的“透明化”管理。
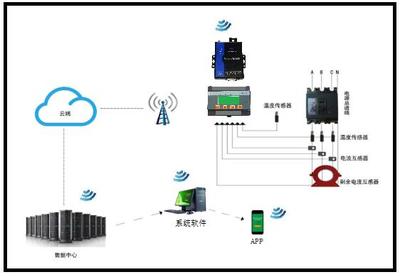
二、AI驅動的智能風險識別與預警。系統內嵌了先進的AI視覺分析算法,能夠對實時視頻流進行毫秒級分析。它不僅能識別煙火、液體泄漏、設備異常振動等傳統風險,更能精準識別人員未佩戴安全裝備、違規闖入危險區域、操作行為不規范等“人因風險”。一旦發現隱患,系統會瞬間觸發多級告警,并通過5G網絡將信息精準推送至現場人員、班組負責人及安全指揮中心,實現從“事后追溯”到“事前預警、事中干預”的根本轉變。
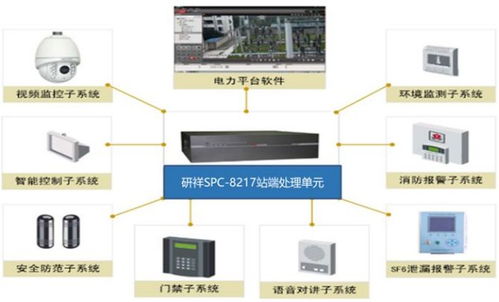
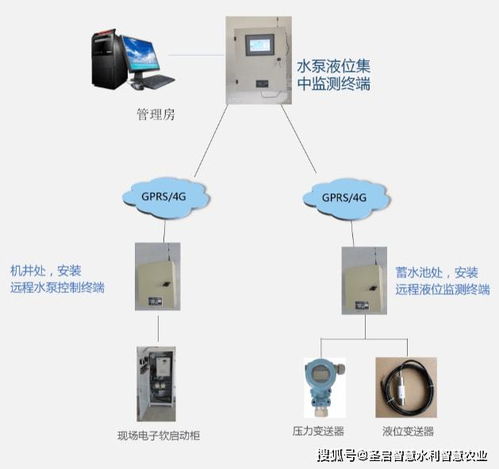
三、數據融合與決策支持。系統并非孤立運行,而是與企業的DCS(分布式控制系統)、設備狀態監測系統、環境監測傳感器等深度集成。通過5G網絡匯聚各類異構數據,在云端構建統一的“安全數據湖”。基于大數據分析,系統能夠評估整體安全態勢,預測設備故障周期,甚至模擬事故演進路徑,為管理者的科學決策提供強有力的數據支撐。
該案例的成功實施,帶來了顯著的經濟與社會效益。據統計,應用企業的事故隱患識別率提升了85%以上,應急響應時間縮短了70%,因安全事故導致的非計劃停機大幅減少,直接經濟效益顯著。更重要的是,它極大保障了一線員工的生命安全,提升了本質安全水平。
此次入選國家能源局優秀案例,標志著寶山在推動5G與實體經濟深度融合、搶占工業互聯網新賽道方面取得了實質性成果。該案例的成功經驗,為能源、化工、鋼鐵等高危行業提供了一條可借鑒的數字化轉型與安全升級路徑。隨著5G-A(5G演進)和6G技術的不斷發展,此類“5G+安全”的應用必將更加深入,為構建更加智慧、堅韌、綠色的現代能源體系注入強勁動能。
如若轉載,請注明出處:http://www.puhg.cn/product/78.html
更新時間:2026-06-02 20:32:30